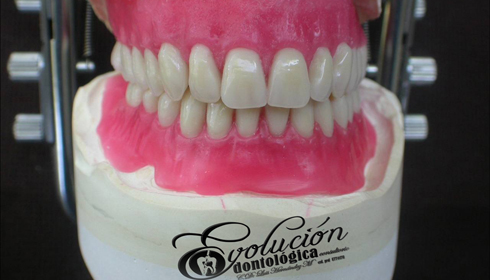
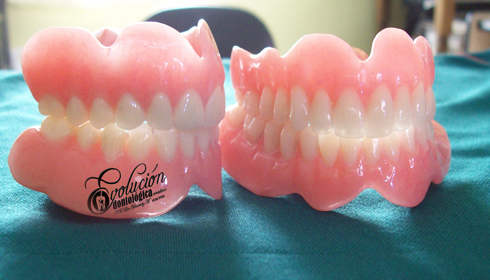
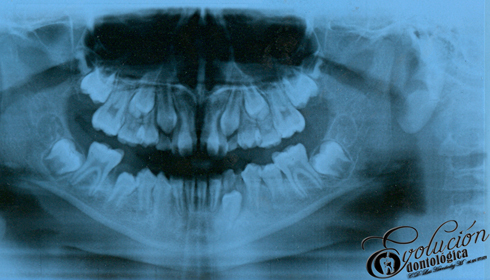
Historia de la odontología (evolucionodontologica)
Historia de la odontología
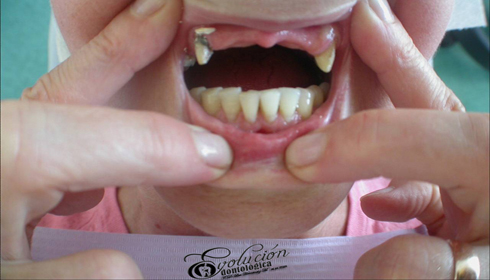
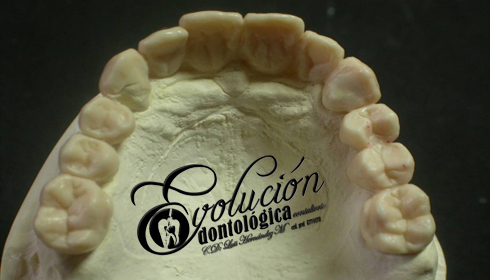
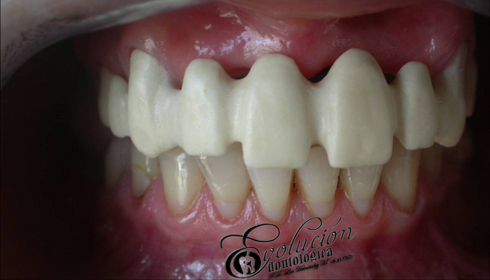
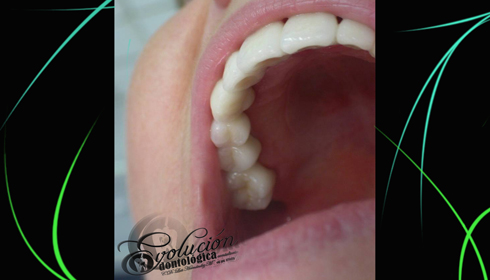
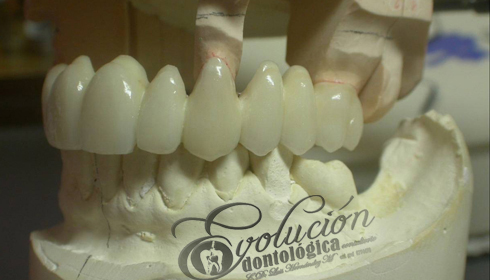
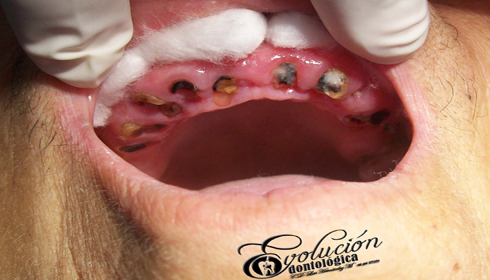
Las enfermedades han aquejado a la humanidad desde sus mismos inicios, en especial el agudo y lancinante dolor dentario producido por una caries profunda o un absceso periapical. Técnicas curativas y rehabilitadoras han sido practicadas por muchos médicos a lo largo de la historia. El registro más antiguo que existe sobre una práctica primitiva egipcia de la Odontología data de hace 5.000 años (3.000 años antes de nuestra era). Hessie-Re es considerado el primer dentista conocido de la historia. Una inscripción egipcia en madera muestra a Hessie-Re como jefe de médicos de la corte. Tiempo después esta profesión fue asumida por los barberos quienes además de los servicios de cortes de cabello, asumían las extracciones dentales de los clientes aquejados de dolor. Luego que comenzaron a ejercer los flebotonianos y cirujanos dentistas en distinta partes del mundo, como parte de las autorizaciones dadas por las autoridades españolas de la época. El francés Pierre Fauchard es considerado el padre de la Odontología Moderna, por sus novedosos aportes a la especialidad.
cancer bucal (evolucion odontologica)
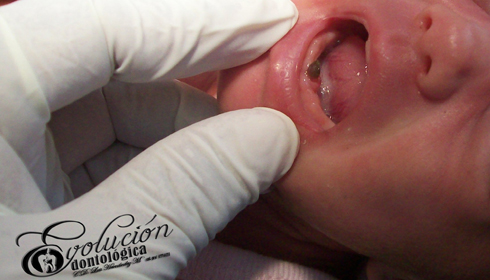
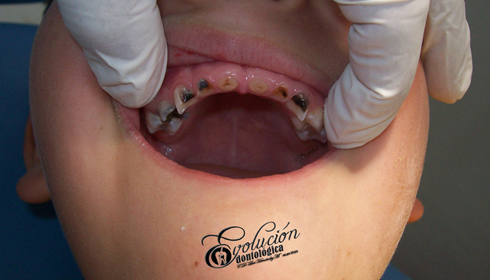
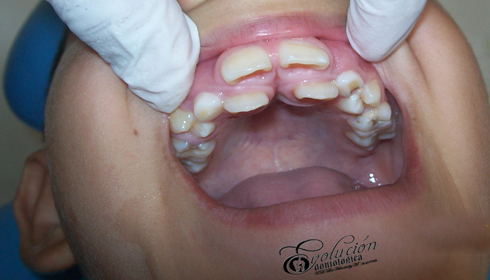
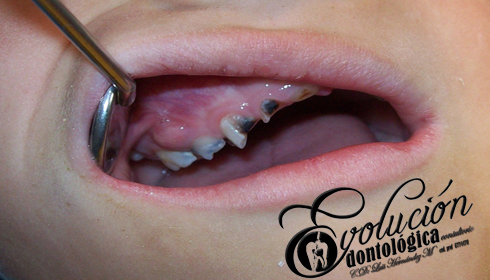
El cáncer bucal se puede formar en cualquier parte de la boca o la garganta. La mayoría de los cánceres bucales comienzan en la lengua y la base de la boca. Cualquier persona puede tener un cáncer bucal, pero el riesgo es más alto en los hombres, mayores de 40 años, fumadores o consumidores de alcohol o en personas con antecedentes de cáncer de cabeza o cuello. La exposición frecuente al sol también es un factor de riesgo de cáncer labial.
Los síntomas del cáncer bucal incluyen:
- Manchas blancas o rojas dentro de la boca
- Una llaga en la boca que no se cura
- Hemorragias en la boca
- Caída de dientes
- Problemas o dolor para tragar
- Un bulto en el cuello
- Dolor de oído
Los tratamientos para el cáncer bucal pueden incluir cirugía, radioterapia o quimioterapia. Algunos pacientes reciben una combinación de tratamientos.
XI Congreso Internacional; De Técnicos Para Técnicos 2011 (evolucion odontologica)
-Enrico Steger, Italia
-Rodrigo Monsano, Brasil
-Joao Carlos Reis, Brasil
-Robert Zubak, República Checa
-Azami Tanaka, Japón
-William Pagan, Estados Unidos
-Kazunobu Yamada, Japón
-Odontólogos y técnicos haciendo equipo, tomando impresiones, preparando, cementando prótesis, ésto y mucho más... en vivo.
- Mesas clínicas con los mejores técnicos y odontólogos del mundo.
- Talleres técnicos (trabaja con los equipos y materiales antes de comprarlos).
El mejor foro internacional con las mejores empresas dentales del mundo. Solamente aquí podrás vivir el lanzamiento al mercado de los nuevos materiales, equipos y técnicas de vanguardia.
APRENDE, COMPARA, PRUEBA Y COMPRA los mejores materiales del mundo.
Auditorio Interdisciplinario
¡Algo que jamás imaginaste! el único foro de debate entre clínicos y técnicos.
Conferencias como nunca las has visto, diseñadas especialmente para ti.
Compra tu boleto ¡AHORA Y AHORRA!
- ALTA TÉCNICA DENTAL
Reúne a los mejores del mundo
Costo real del boleto $800 pesos mexicanos
Aprovecha nuestra promoción de primavera y compra tu boleto durante el mes de marzo por tan sólo $500 pesos mexicanos (público en general)
Precio a suscriptores de la revista $400 pesos mexicanos
Promoción
NO ACUMULABLE
Informes e inscripciones en Alta Técnica Dental:
5523-6107, 5543-0499, 5523-3763, 01800-633-7400
congreso@tecnicadental.com
edicion@tecnicadental.com
altecden@yahoo.com.mx
Migraña (evolucionodontologica)
Algunas personas que padecen mig rañas tienen síntomas de advertencia, llamados aura, antes de que comience el verdadero dolor de cabeza. Un aura es un grupo de síntomas, generalmente alteraciones en la visión, que sirven de signo de advertencia de que se va a presentar un terrible dolor de cabeza. Sin embargo, la mayoría de las personas no presentan tales signos de advertencia.
Ver también:
Causas, incidencia y factores de riesgo
Muchas personas sufren migrañas o jaquecas: aproximadamente 11 de cada 100. Los dolores de cabeza tienden a aparecer primero entre los 10 y los 46 años. Ocasionalmente, las migrañas pueden ocurrir posteriormente en la vida en una persona sin antecedentes de tales dolores de cabeza. Las migrañas pueden ser hereditarias y se presentan con más frecuencia en las mujeres que en los hombres. Las mujeres pueden sufrir menos migrañas cuando están en embarazo. De hecho, la mayoría de las mujeres con tales dolores de cabeza tienen menos ataques durante los últimos dos trimestres del embarazo.
Una migraña es causada por actividad cerebral anormal, desencadenada por estrés, ciertos alimentos, factores medioambientales o algo más. Sin embargo, la cadena exacta de eventos sigue sin aclararse.
Los científicos solían creer que las migrañas se debían a cambios en los vasos sanguíneos dentro del cerebro. En la actualidad, la mayoría de los expertos médicos cree que el ataque realmente comienza en el cerebro mismo, donde involucra varias vías nerviosas y químicos en dicho órgano. Los cambios afectan el flujo sanguíneo en el cerebro y tejidos circundantes.
Los ataques de migraña pueden desencadenarse por:
- Alcohol
- Reacciones alérgicas
- Luces brillantes
- Ciertos olores o perfumes
- Cambios en los niveles hormonales (lo cual puede ocurrir durante el ciclo menstrual de una mujer o con el uso de pastillas anticonceptivas)
- Cambios en los patrones de sueño
- Ejercicio
- Ruidos fuertes
- Saltarse las comidas
- Estrés físico o emocional
- Tabaquismo o exposición al humo del tabaco
Ciertos alimentos y conservantes en los alimentos pueden desencadenar migrañas en algunas personas. Los desencadenantes relacionados con los alimentos pueden abarcar:
- Cualquier alimento procesado, fermentado, adobado o marinado
- Productos horneados
- Chocolate
- Productos lácteos
- Alimentos que contengan glutamato monosódico (GMS)
- Alimentos que contengan tiramina que incluyen el vino rojo, el queso curado, el pescado ahumado, los hígados de pollo, los higos, algunas legumbres)
- Frutas (aguacate, banano, frutos cítricos)
- Carnes que contengan nitratos (como el tocino, los perros calientes, el salami, las carnes curadas)
- Nueces
- Cebollas
- Mantequilla de maní
Es posible que esta lista no incluya todos los desencadenantes.
Las verdaderas jaquecas no son el resultado de un tumor cerebral u otro problema médico serio. Sin embargo, sólo un médico experimentado puede determinar si los síntomas se deben a una migraña u otra afección.
Síntomas
Las alteraciones en la visión o aura se consideran un "signo de advertencia" de que una migraña está por venir. El aura ocurre en ambos ojos y puede involucrar cualquiera de los siguientes aspectos:
- Un punto de ceguera temporal
- Visión borrosa
- Dolor ocular
- Ver estrellas o líneas en zig zag
- Visión de un túnel
No toda persona que padece migrañas presentan un aura. Aquellos que sí normalmente experimentan una alrededor de 10 a 15 minutos antes del dolor de cabeza. Sin embargo, puede ocurrir simplemente desde unos cuantos minutos hasta 24 horas antes. No siempre un dolor de cabeza sigue a un aura.
Las jaquecas pueden ser sordas o severas. El dolor puede sentirse detrás del ojo o en la parte posterior de la cabeza y el cuello. Para muchos pacientes, los dolores de cabeza empiezan en el mismo lado cada vez. Los dolores de cabeza normalmente:
- Se sienten pulsátiles, palpitantes, que laten con violencia
- Son peores en un lado de la cabeza
- Comienzan como un dolor sordo y empeoran en cuestión de minutos a horas
- Duran de 6 a 48 horas
Otros síntomas que se pueden presentar con los dolores de cabeza abarcan:
- Escalofríos
- Aumento de la micción
- Fatiga
- Inapetencia
- Náuseas y vómitos
- Entumecimiento, hormigueo o debilidad
- Problemas para concentrarse, dificultad para encontrar palabras
- Sensibilidad a la luz o al sonido
- Sudoración
Los síntomas pueden persistir aún después de que la migraña desaparece. Los pacientes que padecen migraña algunas veces llaman a esto "resaca" migrañosa. Los síntomas pueden abarcar:
- Sentirse embotado mentalmente, como que el pensamiento no es claro ni brillante
- Aumento de la necesidad de dormir
- Dolor de cuello
Signos y exámenes
El médico puede diagnosticar este tipo de dolor de cabeza haciendo preguntas acerca de los síntomas y los antecedentes de migrañas en la familia. Se hará un examen físico completo para determinar si los dolores de cabeza se deben a tensión muscular, problemas sinusales o a un trastorno cerebral serio.
No hay ningún examen específico para comprobar que el dolor de cabeza sea realmente una migraña. Sin embargo, el médico puede ordenar una resonancia magnética o una tomografía computarizada del cerebro si nunca se las han hecho antes.
Si usted tiene una migraña con síntomas inusuales como debilidad, problemas de memoria o pérdida de la lucidez mental, es posible que se necesite un EEG para descartar convulsiones. Igualmente, se podría realizar una punción lumbar (punción raquídea).
Tratamiento
No existe una cura específica para las jaquecas o migrañas. El objetivo es prevenir los síntomas evitando o alterando los factores desencadenantes.
Una buena manera de identificar los factores desencadenantes es llevar un diario de los dolores de cabeza. Anote:
- Cuándo ocurren los dolores de cabeza
- Qué tan fuertes son
- Qué ha comido
- Qué tanto ha dormido
- Otros síntomas
- Otros factores posibles (las mujeres deben anotar en qué momento de su ciclo menstrual están)
Por ejemplo, el diario puede revelar que sus dolores de cabeza tienden a ocurrir más a menudo en días cuando se despierta más temprano de lo usual. Cambiar su horario de sueño puede producir menos ataques de migraña.
Cuando usted tenga en verdad síntomas de migraña, intente tratarlos de inmediato y así el dolor de cabeza probablemente sea menos intenso. Cuando aparezcan los síntomas de migraña:
- Tome agua para evitar la deshidratación, sobre todo si ha vomitado
- Descanse en una habitación silenciosa y oscura
- Coloque un paño frío sobre la cabeza
Hay muchos medicamentos disponibles para las personas con migraña y se utilizan para:
- Reducir el número de ataques
- Detener la migraña una vez que se presentan los primeros síntomas
- Tratar el dolor y otros síntomas
REDUCIR LOS ATAQUES
Si usted padece migrañas frecuentes, el médico puede prescribirle medicamentos para reducir el número de ataques. Es necesario tomarlos todos los días para que sean efectivos y pueden abarcar:
- Antidepresivos como la amitriptilina
- Medicamentos para la presión arterial, como betabloqueadores (propanolol) o bloqueadores de los canales del calcio (verapamilo)
- Medicamentos anticonvulsivos como ácido valproico, gabapentina y topiramato
- Inhibidores selectivos de la recaptación de la serotonina (ISRS) como venlafaxina
- Inhibidor selectivo de la captación de norepinefrina (SNRI) como duloxetina
DETENER UN ATAQUE
Otros medicamentos se toman ante el primer signo de un ataque de migraña. Los analgésicos de venta libre como el acetaminofeno (paracetamol), el ibuprofeno o el ácido acetilsalicílico (aspirin) a menudo ayudan, especialmente cuando la migraña es leve. Si no ayudan, solicítele al médico que le recete medicamentos. (Sin embargo, tenga en cuenta que el uso excesivo o el mal uso de tales analgésicos puede ocasionar cefaleas de rebote. Las cefaleas de rebote crónicas típicamente ocurren en personas que toman analgésicos más de tres días a la semana de manera regular).
Entre los diferentes tipos de medicamentos, el médico puede seleccionar:
- Triptanos, los medicamentos que se recetan con mayor frecuencia para detener los ataques de migraña, como sumatriptán (Imitrex), rizatriptán (Maxalt), almotriptán (Axert), frovatriptán (Frova) y zolmitriptán (Zomig)
- Derivados del cornezuelo de centeno como la dihidroergotamina o la ergotamina con cafeína (Cafergot)
- Isometepteno (Midrin)
Estos medicamentos vienen en formas diferentes. A los pacientes que tengan náuseas y vómitos con sus migrañas se les puede prescribir un aerosol nasal, supositorio o inyección en lugar de las píldoras.
Algunos medicamentos para la migraña constriñen los vasos sanguíneos y no se deben emplear si usted está en riesgo de sufrir ataques cardíacos o tiene cardiopatía, a menos que el médico haya dado otras instrucciones. El cornezuelo de centeno no se debe consumir si usted está embarazada o planeando quedar en embarazo, debido a que puede causar efectos secundarios serios en un bebé nonato.
TRATAMIENTO DE LOS SÍNTOMAS
Se administran otros medicamentos principalmente para tratar los síntomas de migraña. Usados solos o en combinaciones, estos fármacos pueden reducir el dolor, las náuseas o la angustia emocional. Los medicamentos en este grupo abarcan:
- Medicamentos antinauseosos como la procloroperacina
- Analgésicos de venta libre como el acetaminofeno o paracetamol (Tylenol)
- Sedantes como el butalbital
- Analgésicos narcóticos como la meperidina
- Antinflamatorios no esteroides (AINES) como el ibuprofeno
Si usted quiere considerar una alternativa, la matricaria es una hierba popular para las migrañas. Algunos estudios, no todos, apoyan el uso de esta hierba para el tratamiento de las migrañas. Si desea probarla, asegúrese primero de que el médico lo apruebe. Sepa también que los medicamentos herbales que se venden en las droguerías y en las tiendas naturistas no están regulados, por lo tanto consulte con un especialista en medicina natural para seleccionar hierbas.
Grupos de apoyo
American Council for Headache Education: www.achenet.org
The National Migraine Association: www.migraines.org
National Headache Foundation: www.headaches.org
Expectativas (pronóstico)
Cada paciente responde de manera diferente al tratamiento. Algunos pacientes presentan dolores de cabeza muy poco frecuentes que requieren poco o ningún tratamiento, mientras que otros requieren el uso de numerosos medicamentos o incluso una hospitalización ocasional.
Complicaciones
Las migrañas o jaquecas son un factor de riesgo de accidente cerebrovascular tanto en hombres como en mujeres.
Estas migrañas o jaquecas normalmente no representan una amenaza significativa para la salud general. Sin embargo, pueden ser un problema prolongado (crónico) y pueden interferir con su diario vivir.
Situaciones que requieren asistencia médica
Llame al número local de emergencias (911 en los Estados Unidos) si:
- Está experimentando "el peor dolor de cabeza de la vida".
- Presenta problemas del habla, la visión, el movimiento o pérdida del equilibrio, especialmente si no ha tenido estos síntomas con una migraña antes.
- Los dolores de cabeza son más intensos al acostarse.
- Los dolores de cabeza comienzan de manera muy repentina.
También llame al médico si:
- Los patrones del dolor de cabeza o el dolor cambian.
- Los tratamientos que alguna vez funcionaron ya no sirven.
- Presenta efectos secundarios de los medicamentos, incluyendo latidos cardíacos irregulares, piel pálida o azul, somnolencia extrema, tos persistente, depresión, fatiga, náuseas, vómitos, diarrea, estreñimiento, dolor de estómago, calambres, resequedad en la boca o demasiada sed.
- Está embarazada o podría quedar en embarazo, dado que algunos medicamentos no deben tomarse en este estado.
Prevención
El hecho de entender los desencadenantes del dolor de cabeza puede ayudarle a evitar los alimentos y situaciones que causan sus migrañas. Mantenga un diario de los dolores de cabeza para ayudar a identificar la fuente o el desencadenante de los síntomas. Luego modifique su ambiente o hábitos para evitar dolores de cabeza futuros.
Otros consejos para prevenir las migrañas son:
- Evitar el cigarrillo
- Evitar el alcohol
- Evitar los edulcorantes artificiales y otros desencadenantes relacionados con los alimentos
- Hacer ejercicios regularmente
- Dormir bien cada noche
- Aprender a relajarse y a reducir el estrés: algunos pacientes han descubierto que la biorretroalimentación y la autohipnosis ayudan a reducir el número de ataques de migraña
Nombres alternativos
Jaqueca
Referencias
Wilson JF. In the clinic: migraine. Ann Intern Med. 2007;147(9):ITC11-1-ITC11-16.
Ebell MH. Diagnosis of migraine headache. Am Fam Physician. 2006;74(12):2087-2088.
Detsky ME, McDonald DR, et al. Does this patient with headache have a migraine or need neuroimaging? JAMA. 2006;296(10):1274-1283.
Lipton RB, Bigal ME, Steiner TJ, Silberstein SD, Olesen J. Classification of primary headaches. Neurology. 2004;63(3):427-435.
Silberstein SD, Young WB. Headache and facial pain. In: Goetz CG. Textbook of Clinical Neurology. 3rd ed. St. Louis, Mo: WB Saunders; 2007:chap. 53.
Actualizado: 12/21/2009
Versión en inglés revisada por: Daniel B. Hoch, PhD, MD, Assistant Professor of Neurology, Harvard Medical School, Department of Neurology, Massachusetts General Hospital. Also reviewed by David Zieve, MD, MHA, Medical Director, A.D.A.M., Inc.
Traducción y localización realizada por: DrTango, Inc.
'El peor dolor del mundo' (evolucion odontologica)
El mismo médico que en el siglo II hizo una de las primeras descripciones de la migraña, fue el primero en describir unos atípicos dolores de cabeza en los que "tenían lugar espasmos y distorsiones del semblante". Hasta el siglo XVIII, este incapacitante trastorno no recibiría el nombre de 'tic doloroso'. Es lo que hoy se conoce como neuralgia del trigémino, el motivo más frecuente de neuralgia facial.
Las personas con neuralgia del trigémino, uno de los 12 pares de nervios que recorren la cabeza, definen sus síntomas como 'El peor dolor del mundo'. El llamado 'tic doloroso' es un dolor facial extremadamente intenso, una suerte de espasmo que se da en el pómulo o en la mandíbula. Una revisión publicada en el último número del 'British Medical Journal' repasa algunos aspectos de esta incapacitante enfermedad:
Síntomas
Un corrientazo en un lado de la cara. Puede que dure unos segundos, o se prolongue varios interminables minutos. Este es el síntoma más característico de las neuralgias del trigémino, tal y como las describen sus pacientes, habitualmente mujeres y mayores de 50 años.
Aunque las crisis son breves, suelen reaparecer durante varios días, semanas e incluso meses. Como media, estos ataques duran 49 días. Aunque el paciente puede estar mucho tiempo sin sufrir un nuevo ataque, lo habitual es que reaparezcan. De acuerdo con un estudio realizado sobre la evolución de la enfermedad, la mayoría de los pacientes tendrá más de un ataque a lo largo de su vida: el 19% presentará dos, el 24% tres y en 28% cuatro o más.
Los ataques pueden ser espontáneos o desencadenarse tras tocar diferentes zonas de la cara (puntos gatillo), por ejemplo con actividades tan simples como cepillarse los dientes, afeitarse o aplicar maquillaje. A veces el dolor es tan intenso que impide comer o beber.
Causas
Existen múltiples teorías sobre las causas de esta dolencia. Según la revisión del 'British', entre el 80% y 90% de las neuralgias del trigémino llamadas idiopáticas (es decir, que en teoría no tienen causa conocida) se deben en realidad a la compresión del nervio, cerca de su salida del tronco encefálico, por una vena o arteria que formen un 'bucle'.
Los demás casos pueden deberse a otro tipo de pinzamiento nervioso (por ejemplo, a causa de un tumor benigno o de un quiste), a la esclerosis múltiple o a un infarto cerebral que haya afectado la parte inferior del cerebro, por donde penetra el nervio.
Diagnóstico
Muchas veces, el correcto diagnóstico se retrasa, solapado por otras dolencias faciales más frecuentes, como un dolor dental o una migraña. No existen pruebas específicas para esta neuralgia, así que el diagnóstico es clínico. Es decir, para diagnosticar el problema hace falta un examen físico y el historial médico (descripción del dolor, antecedentes familiares...).
Sin embargo, también se realizan otras pruebas, para descartar otros problemas. Será necesario realizar una radiografía dental para descartar problemas odontológicos. El escáner cerebral también puede ayudar a descartar otras posibles causas del dolor o, incluso, identificar un problema que esté afectando al trigémino (un tumor, una esclerosis múltiple). Los autores creen necesaria una resonancia en pacientes jóvenes, aquellos con síntomas atípicos (como, por ejemplo, pérdida sensorial) y los que no respondan a la terapia médica inicial.
Tratamiento
La neuralgia del trigémino causa un dolor grave que no responde a los analgésicos clásicos. Aunque se han hecho muy pocos estudios sobre el tratamiento de esta neuralgia, existen algunas claves sobre cómo aliviar estos ataques.
FÁRMACOS
- Carbamazepina: este antiepiléptico es el fármaco de elección para la neuralgia trigeminal, pues ha demostrado su eficacia en diferentes estudios. Sin embargo, muchos pacientes deben abandonarlo debido a sus frecuentes efectos secundarios, como vértigos, cefaleas y otros efectos sobre el sistema nervioso, trastornos gastrointestinales (náuseas, vómitos) y reacciones alérgicas cutáneas.
- Antiepilépticos de nueva generación: si el paciente se ve obligado a dejar la carbamazepina por sus efectos secundarios, los autores aconsejan probar con oxcarbazepina (muy similar al anterior, aunque suele tolerarse mejor) y con la gabapentina (que ha demostrado ser eficaz en otro tipo de dolores de origen neurológico). Lamotrigina o baclofeno (para el tratamiento de la esclerosis múltiple) también podrían resultar eficaces, de acuerdo con pequeños estudios. También puede recurrirse a otros anticonvulsivos como fenitoína, clonazepam o valproato.
- Tratamiento combinado: si la carbamazepina no resulta eficaz, los autores recomiendan añadir un segundo fármaco o cambiar de medicamento, pasándose a alguna de las alternativas mencionadas.
Si fallan todos estos fármacos, los autores recomiendan que se revise el diagnóstico (valorando otras posibles causas del dolor facial) y que se consideren las opciones quirúrgicas.
CIRUGÍA
Existen dos intervenciones disponibles:
- Descompresión microvascular: se explora la fosa posterior (un pequeño espacio en el cráneo, cerca del tronco encefálico y el cerebelo) y se separa el nervio trigémino del vaso sanguíneo que lo está comprimiendo. La intervención ha demostrado tener buenos resultados en pacientes con una neuralgia trigeminal clásica, de corta duración y sin cirugía previa. Según la revisión del 'British', esta es la técnica que ofrece mejores resultados a largo plazo, aunque el paciente debe tener en cuenta que sus riesgos son mayores (de complicaciones importantes e, incluso, de fallecer, aunque, en términos absolutos, este riesgo es muy bajo: en torno al 0,4% de los intervenidos fallecen).
- Tratamientos ablativos: se trata de intervenciones que lesionan el trigémino de diferentes formas, como inyectando glicerol o destruyendo las fibras transmisoras de la señal dolorosa mediante calor (termocoagulación) o una corriente eléctrica. Aunque son menos eficaces a largo plazo y pueden producir complicaciones menores, tienen mucho menor riesgo de complicaciones importantes, de acuerdo con la revisión. Son recomendables en pacientes de riesgo o en aquellos con una enfermedad atípica. Por ejemplo, funciona bien en personas con entumecimiento facial, un síntoma poco frecuente en la neuralgia del trigémino.
Otro tratamiento que 'daña' el trigémino es la radiocirugía, indicada en personas con problemas médicos que no pueden ser intervenidas y en las que han fallado otras intervenciones ablativa
Mascarillas - INSTRUMENTACIÓN PARA EL MANEJO DE LA VÍA AÉREA (evolucion odontologica)

INSTRUMENTACIÓN PARA EL MANEJO
DE LA VÍA AÉREA
|
|
|
|
Existe otra serie de equipo auxilar como protectores dentales, fórceps para intubación, catéter de aspiración, lubricantes, etc.
LA MÁQUINA DE ANESTESIA
|
|
|
|
|
- a) Complejidad. Son obvios los peligros del mal funcionamiento de un dispositivo complicado, por lo que los sencillos suelen ser seguros y más prácticos.
- a) Superficie de gasa.
- a) Se basan en el movimiento de aire que ocasiona la respiración.
- a) Con plancha de calentamiento eléctrico.
- a) Vaporizador de éter de Edison; el calor de absorción proviene de carbón activado.
|
VAPORIZADORES
|
EBULLICIÓN
|
|
|
DE DESFLURANO
|
Y VELOCIDAD DE FLUJO DE GAS FRESCO
VENTILACIÓN MECÁNICA
Y HUMIDIFICACIÓN EN ANESTESIA
|
|
|
|
|
|
MONITOREO EN ANESTESIA
|
LA ARTERIA PULMONAR
|
|
|
|
|
|
|
|
|
El monitoreo hemodinámico ha de basarse fisiológicamente y orientarse hacia una meta definida.